Los datos iniciales del estudio FIBRONEER™-ILD (enfermedades pulmonares intersticiales, por sus siglas en inglés) muestran que el medicamento oral en investigación: Nerandomilast, cumplió el criterio de valoración principal, al mejorar la función pulmonar
Avances en tratamiento de Fibrosis Pulmonar Progresiva
Boehringer Ingelheim anunció que su estudio FIBRONEER™-ILD alcanzó su criterio de valoración principal al demostrar que la molécula Nerandomilast ofrece mejoría en la capacidad pulmonar al reportar el cambio sustancial respecto al valor basal en la capacidad vital forzada (CVF) en la semana 52 comparado con placebo. La CVF es una medida clave para determinar la función pulmonar.[i]
Nerandomilast es un tratamiento oral en investigación que actúa como inhibidor de la enzima PDE4B.[ii] Este fármaco forma parte del programa global FIBRONEER™, que incluye dos ensayos clínicos avanzados de Fase III: FIBRONEER™-IPF [iii], enfocado en pacientes con Fibrosis Pulmonar Idiopática (FPI), y FIBRONEER™-ILD[iv] , dirigido a pacientes con Fibrosis Pulmonar Progresiva (FPP).
Los datos iniciales de los ensayos indican que Nerandomilast tiene un perfil de seguridad y tolerancia consistente con estudios anteriores y efectos secundarios similares al placebo[v]. Este tratamiento oral está diseñado para ayudar a personas con Fibrosis Pulmonar Progresiva y Fibrosis Pulmonar Idiopática.
Con base en estos resultados, Boehringer Ingelheim planea presentar la solicitud para la aprobación de este nuevo fármaco a la FDA en Estados Unidos y otras autoridades internacionales para el tratamiento de la FPP.
Boehringer Ingelheim destacó el potencial de Nerandomilast como tratamiento para la Fibrosis Pulmonar Progresiva, basándose en los resultados iniciales positivos del estudio FIBRONEER™-ILD.
«Estamos observando un perfil de seguridad y tolerancia que podría ayudar a hacer frente a los retos del tratamiento de la FPP», comentó Shashank Deshpande, responsable de Salud Humana y miembro del Consejo de Administración de Boehringer Ingelheim.
Deshpande subrayó que los avances en el programa FIBRONEER™ reafirman el compromiso de la compañía con mejorar la calidad de vida de los pacientes que enfrentan esta enfermedad debilitante y consolidan su liderazgo en la investigación de la fibrosis pulmonar.
Acerca de FIBRONEER™-ILD [vi]
El estudio FIBRONEER™-ILD es un ensayo clínico diseñado para evaluar la seguridad y eficacia de Nerandomilast, una molécula en investigación en pacientes con fibrosis pulmonar progresiva (FPP). Este estudio, que duró al menos 52 semanas, incluyó un enfoque doble ciego y aleatorio, comparando Nerandomilast en dos dosis (9 mg y 18 mg) dos veces al día contra placeboii.
El criterio de valoración primario fue medir los cambios en la capacidad pulmonar (CVF) a lo largo del tiempo, mientras que el criterio de valoración secundario fue analizar eventos como exacerbaciones pulmonares graves, hospitalizaciones por causa respiratoria o fallecimiento durante la realización del ensayo.
En total, participaron 1,178 pacientes de más de 40 países en más de 400 centros médicos, lo que refuerza el carácter global de este esfuerzo científico.
México participo en la conducción de los dos estudios que conforman el programa FIBRONEER™, siendo uno de los países más relevantes en Latinoamérica en cuanto a la participación de pacientes. A través del esfuerzo conjunto de 7 centros expertos en investigación clínica distribuidos en diferentes estados de la república mexicana, se logró incrementar en un 196% la participación de pacientes mexicanos en el desarrollo de estas terapias innovadoras.
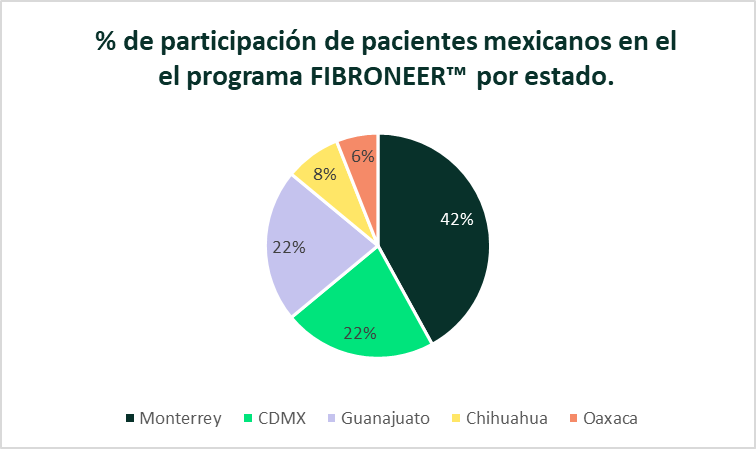
El Hospital Universitario Dr. José Eleuterio González en Monterrey, Nuevo León, se destacó como uno de los principales contribuidores al éxito en la participación de México en el programa FIBRONEER™, puesto que el 42% de pacientes mexicanos que participaron en el programa, lo hicieron en este centro de investigación. El programa FIBRONEER™ en México abarcó el periodo de julio de 2023 a marzo de 2025. La distribución geográfica de los pacientes mexicanos que participaron se muestra a continuación:
Acerca del programa clínico FIBRONEER™
El programa FIBRONEER™ incluye dos estudios Fase III: FIBRONEER™-IPF[vii], enfocado en pacientes con Fibrosis Pulmonar Idiopática (FPI), y FIBRONEER™-ILD[viii], dirigido a pacientes con Fibrosis Pulmonar Progresiva (FPP). Ambos estudios son aleatorizados, doble ciego y controlados con placebo, con una duración mínima de 52 semanas.
En ambos ensayos, el criterio de valoración primario es el cambio absoluto con respecto al valor basal en la CVF (ml) tras 52 semanas de tratamiento. El criterio de valoración secundario clave es el tiempo transcurrido hasta la primera aparición de cualquiera de los componentes del criterio de valoración compuesto: tiempo hasta la primera exacerbación aguda de la FPI, la primera hospitalización por causa respiratoria o muerte durante los ensayos.
Acerca de nerandomilast [ix] ,[x] , [xi]
Nerandomilast actúa como inhibidor de la enzima PDE4B en fase de investigación que está evaluando su eficacia para la Fibrosis Pulmonar Idiopática (FPI) y la Fibrosis Pulmonar Progresiva (FPP). Hasta el momento, su uso no está aprobado y sigue siendo un agente en investigación.
En febrero de 2022, la FDA otorgó a Nerandomilast la designación de «terapia innovadora» para tratar la FPI, destacando su potencia.[xii]
La eficacia, seguridad y tolerabilidad de Nerandomilast se estudió en un ensayo Fase II aleatorizado, doble ciego y controlado con placebo realizado e 147 pacientes con FPI. El criterio de valoración primario fue un cambio respecto al valor basal en la CVF durante un periodo de tratamiento de 12 semanas.[xiii]
La Fibrosis Pulmonar Idiopática (FPI) es una de las enfermedades pulmonares intersticiales fibrosantes progresivas más comunes.[xiv] Sus principales síntomas son dificultad para respirar al realizar actividades físicas, tos seca, fatiga y debilidad. [xv]Aunque se clasifica como una enfermedad rara, afecta a unos
3 millones de personas en el mundo, principalmente a hombres mayores de 50 años.[xvi]
Pacientes con enfermedades pulmonares intersticiales (EPI) fibrosantes, distintas de la FPI, pueden desarrollar un fenotipo progresivo conocido como Fibrosis Pulmonar Progresiva (FPP). Esta condición se caracteriza por un empeoramiento de los síntomas respiratorios, un deterioro de la función pulmonar y cambios visibles en las pruebas fisiológicas y radiológicas de la enfermedad. [xvii]
La Fibrosis Pulmonar Progresiva puede causar daños irreversibles en los pulmones y provocar une mortalidad precoz.[xviii]
El diagnóstico de Fibrosis Pulmonar
requiere de una evaluación realizada por un equipo multidisciplinar compuesto
por neumólogos, radiólogos y patólogos expertos en el diagnóstico y manejo de
las enfermedades pulmonares intersticiales.[xix]
[i] Maher TM, et al. (2023) Design of a phase III, double-blind, randomised, placebo-controlled trial of BI 1015550 in patients with
fibrosis pulmonar progresiva (FIBRONEER-ILD). En: BMJ Open Respir Res 2023;10:e001580.
[ii] Richeldi L, et al. (2022) Trial of a Preferential Phosphodiesterase 4B Inhibitor for Idiopathic Pulmonary Fibrosis. In: N Engl J Med 2022;386:2178-2187.
[iii] Boehringer Ingelheim (2024) A Study to Find Out Whether BI 1015550 Improves Lung Function in People With Idiopathic Pulmonary Fibrosis (IPF). Accessed January 2025. Disponible en: https://clinicaltrials.gov/study/NCT05321069
[iv] Boehringer Ingelheim (2024) A Study to Find Out Whether BI 1015550 Improves Lung Function in People With Progressive Fibrosing Interstitial Lung Diseases (PF-ILDs). Consultado en enero de 2025. Disponible en: https://clinicaltrials.gov/study/NCT05321082?tab=results.
[v] Richeldi L, et al. (2022) Trial of a Preferential Phosphodiesterase 4B Inhibitor for Idiopathic Pulmonary Fibrosis. In: N Engl J Med 2022;386:2178-2187.
[vi] Boehringer Ingelheim (2024) A Study to Find Out Whether BI 1015550 Improves Lung Function in People With Progressive Fibrosing Interstitial Lung Diseases (PF-ILDs). Consultado en enero de 2025. Disponible en: https://clinicaltrials.gov/study/NCT05321082?tab=results.
[vii] Boehringer Ingelheim (2024) A Study to Find Out Whether BI 1015550 Improves Lung Function in People With Idiopathic Pulmonary Fibrosis (IPF). Accessed January 2025. Disponible en: https://clinicaltrials.gov/study/NCT05321069
[viii] Boehringer Ingelheim (2024) A Study to Find Out Whether BI 1015550 Improves Lung Function in People With Progressive Fibrosing Interstitial Lung Diseases (PF-ILDs). Consultado en enero de 2025. Disponible en: https://clinicaltrials.gov/study/NCT05321082?tab=results.
[ix] Richeldi L, et al. (2022) Trial of a Preferential Phosphodiesterase 4B Inhibitor for Idiopathic Pulmonary Fibrosis. In: N Engl J Med 2022;386:2178-2187.
[x] Boehringer Ingelheim (2024) A Study to Find Out Whether BI 1015550 Improves Lung Function in People With Idiopathic Pulmonary Fibrosis (IPF). Accessed January 2025. Disponible en: https://clinicaltrials.gov/study/NCT05321069
[xi] Boehringer Ingelheim (2024) A Study to Find Out Whether BI 1015550 Improves Lung Function in People With Progressive Fibrosing Interstitial Lung Diseases (PF-ILDs). Consultado en enero de 2025. Disponible en: https://clinicaltrials.gov/study/NCT05321082?tab=results.
[xii] Boehringer Ingelheim (2022) FDA Grants BI 1015550 Breakthrough Therapy Designation for Idiopathic Pulmonary Fibrosis. Consultado en enero de 2025. Disponible en: https://www.boehringer-ingelheim.com/us/human-health/lung-diseases/pulmonary-fibrosis/fda-grants-bi-1015550-breakthrough-therapy.
[xiii] Richeldi L, et al. (2022) Trial of a Preferential Phosphodiesterase 4B Inhibitor for Idiopathic Pulmonary Fibrosis. In: N Engl J Med 2022;386:2178-2187.
[xiv] Sauleda J, et al. Idiopathic Pulmonary Fibrosis: Epidemiology, Natural History, Phenotypes. Med Sci (Basilea). 2018 Nov 29;6(4):110. doi: 10.3390/medsci6040110. PMID: 30501130; PMCID: PMC6313500.
[xv] European Lung Foundation (2023) IPF – Idiopathic Pulmonary Fibrosis. Consultado en enero de 2025. Disponible en: https://europeanlung.org/en/information-hub/factsheets/ipf-idiopathic-pulmonary-fibrosis/
[xvi] Koudstaal T, et al. (2023) Idiopathic pulmonary fibrosis. En: Presse Med 2023; 52(3):104166
[xvii] Cottin, V. et al. (2023) Criteria for Progressive Pulmonary Fibrosis: Getting the Horse Ready for the Cart. En: Am J Respir Crit Care Med 2023; 207(1):11-13
[xviii] Brown KK, Martinez FJ, Walsh SLF, Thannickal VJ, Prasse A, Schlenker-Herceg R, et al. The natural history of progressive fibrosing interstitial lung diseases. Eur Respir J 2020;55:2000085.
[xix] Raghu G, et al. Diagnosis of Idiopathic Pulmonary Fibrosis. An Official ATS/ERS/JRS/ALAT Clinical Practice Guideline. American Journal of Respiratory and Critical Care Medicine. 2018;198(5), pp.e44-e68.



